Liquid Biopsy
Die Liquid Biopsy (Flüssigbiopsie) beim Prostatakrebs ist ein vielversprechendes,
nicht-invasives Verfahren, das Blut- oder Urinproben nutzt,
um zirkulierende Tumorzellen (CTCs) oder Tumor-DNA (ctDNA) nachzuweisen.
Sie dient hauptsächlich zur Überwachung des Krankheitsverlaufs,
Erkennung von Resistenzen und Therapiesteuerung bei fortgeschrittenem Krebs,
ersetzt jedoch bisher nicht die initiale Gewebebiopsie
Liquid Biopsy
Die Spurensuche nach Krebs-DNA im Blut beim Prostatakarzinom
Die Diagnose eines Prostatakarzinoms stellt für Männer eine Zäsur dar, die nicht nur medizinische, sondern auch tiefe emotionale Fragen aufwirft. Über Jahrzehnte hinweg stützte sich die Urologie auf zwei Säulen: den PSA-Wert und die Gewebestanze. Doch während der PSA-Wert oft unspezifisch ist und auch bei gutartigen Entzündungen steigen kann, empfinden viele Patienten die Biopsie durch den Enddarm oder den Damm als schmerzhaft und belastend. In diese Lücke tritt eine revolutionäre Technologie, die den genetischen Fingerabdruck des Tumors direkt aus einer einfachen Blutprobe isoliert: die Liquid Biopsy. Diese „Flüssigbiopsie“ verspricht eine neue Ära der Präzisionsmedizin, in der nicht mehr das Skalpell, sondern die hochsensitive Analyse von Erbgutfragmenten im Blut den Weg zur optimalen Therapie weist. Für den Patienten bedeutet dies den Verzicht auf riskante Eingriffe bei gleichzeitigem Gewinn an molekularer Information, die eine herkömmliche Biopsie oft gar nicht liefern kann.
Der genetische Fingerabdruck im Blutstrom: Zellen und DNA auf der Flucht
Um zu verstehen, wie ein einfacher Bluttest Informationen über einen Tumor in der Prostata oder in fernen Knochenmetastasen liefern kann, muss man die Biologie des Krebswachstums betrachten. Ein Tumor ist kein isoliertes Gebilde; er steht in ständigem Austausch mit seiner Umgebung. Während Krebszellen wachsen und sich teilen, gehen andere Zellen zugrunde – ein Prozess, den Mediziner als Apoptose (programmierter Zelltod) oder Nekrose (Zelltod durch Schädigung) bezeichnen. Bei diesem Zerfall setzen die Zellen ihre inneren Bausteine frei, darunter auch ihre Erbinformation, die DNA. Da Tumorgewebe oft stark von Blutgefäßen durchzogen ist, gelangen diese winzigen Erbgutschnipsel direkt in den Blutkreislauf.
ctDNA und CTCs: Die unterschiedlichen Boten des Krebses
In der Liquid Biopsy fahnden Spezialisten nach zwei wesentlichen Akteuren, die unterschiedliche Informationen über die Erkrankung preisgeben.
ctDNA (zirkulierende Tumor-DNA): Dies sind freischwimmende Bruchstücke des Erbguts der Krebszellen. Sie sind sehr klein und oft nur für wenige Stunden im Blut nachweisbar, bevor der Körper sie abbaut. Dennoch enthalten sie alle relevanten Mutationen des Tumors. Die Analyse der ctDNA ermöglicht es, gezielt nach genetischen Fehlern zu suchen, für die es bereits hochwirksame Medikamente gibt.
CTCs (zirkulierende Tumorzellen): Im Gegensatz zur ctDNA handelt es sich hierbei um ganze, intakte Krebszellen, die sich vom Haupttumor gelöst haben und im Blut wandern, um an anderer Stelle im Körper neue Metastasen zu bilden. Da diese Zellen „leben“, können Forscher an ihnen nicht nur das Erbgut, sondern auch die Aktivität bestimmter Gene und Proteine untersuchen.
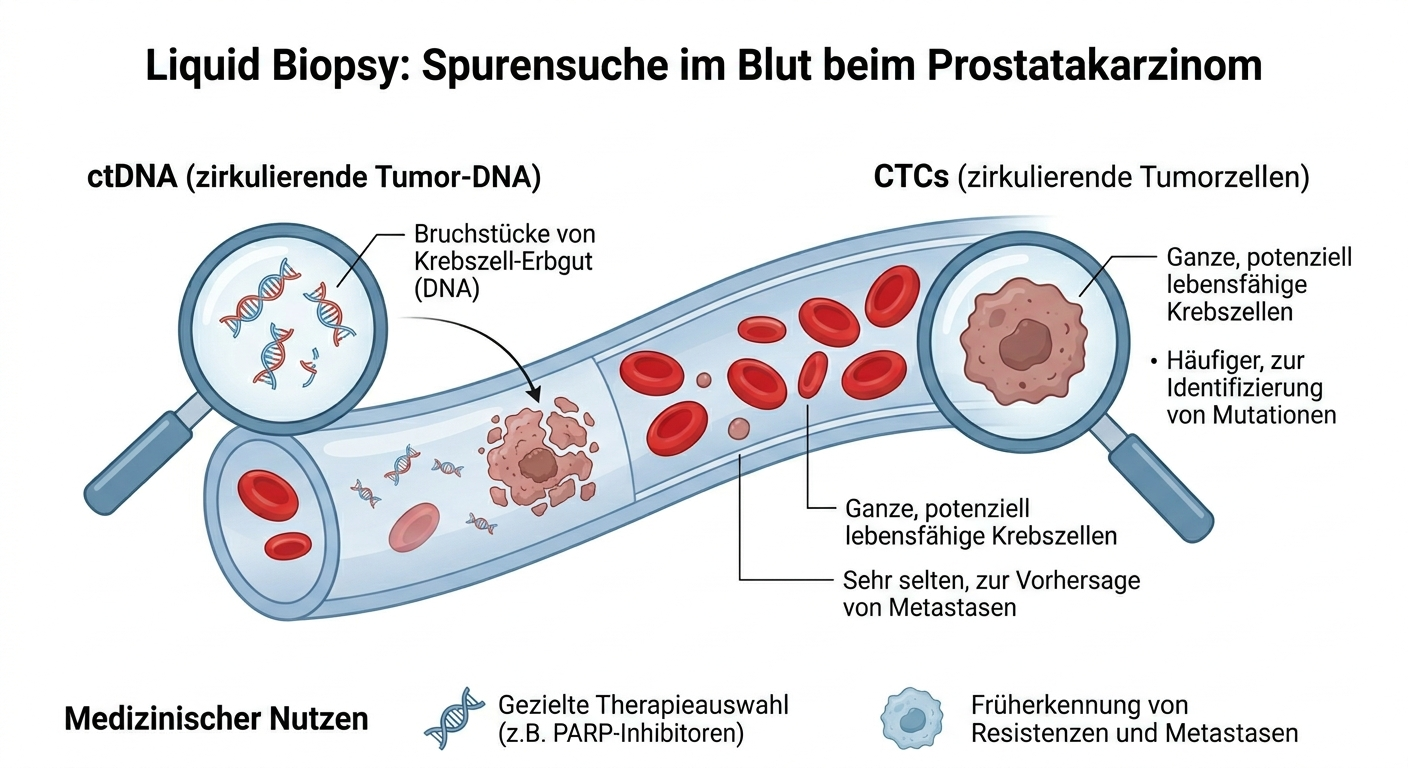
 Der Vergleich: ctDNA versus CTCs
Der Vergleich: ctDNA versus CTCsUm zu verstehen, welche Informationen die Liquid Biopsy liefern kann, muss man zwischen zwei verschiedenen Boten des Krebses unterscheiden:
- ctDNA (zirkulierende Tumor-DNA):
- Natur: Dabei handelt es sich um Erbgutfragmente von bereits verstorbenen Krebszellen.
- Häufigkeit: Diese Fragmente kommen im Blut häufiger vor, besonders wenn eine hohe Tumorlast vorliegt.
- Hauptnutzen: Sie dient vor allem dem Nachweis spezifischer Mutationen, um zielgerichtete Therapien (wie z. B. PARP-Inhibitoren) auszuwählen.
- Technologie: Die Analyse erfolgt mittels hochmoderner Sequenzierungsmethoden (Next-Generation Sequencing, kurz NGS).
- Sensitivität: Das Verfahren ist insbesondere in fortgeschrittenen Krankheitsstadien sehr treffsicher.
- CTCs (zirkulierende Tumorzellen):
- Natur: Dies sind ganze, potenziell noch lebensfähige Krebszellen, die im Blut wandern.
- Häufigkeit: Sie sind extrem selten; man findet oft nur eine einzige dieser Zellen unter etwa einer Milliarde normaler Blutzellen.
- Hauptnutzen: Sie werden genutzt, um die Bildung von Metastasen vorherzusagen und drohende Resistenzen frühzeitig zu erkennen.
- Technologie: Die Zellen müssen aufwendig angereichert und anschließend unter dem Mikroskop analysiert werden.
- Sensitivität: Die Genauigkeit hängt stark von der vorhandenen Zellmenge ab (ein bekanntes System hierfür ist z. B. CellSearch).
Das Problem der Tumorheterogenität lösen
Ein zentraler Grund, warum die Liquid Biopsy oft ein vollständigeres Bild liefert als eine herkömmliche Gewebestanze, liegt in der sogenannten Tumorheterogenität. Ein Prostatakarzinom ist im fortgeschrittenen Stadium oft kein einheitlicher Gegner mehr. Die Zellen in der Prostata können genetisch völlig anders beschaffen sein als die Zellen in einer Metastase im Beckenknochen oder in der Leber. Eine Gewebeprobe entnimmt immer nur Material von einem einzigen Punkt. Würde man nur diesen Punkt untersuchen, könnte man Mutationen in anderen Metastasen übersehen, die den Patienten resistent gegen die geplante Therapie machen. Da jedoch alle Metastasen ihre DNA in dasselbe Blut abgeben, wirkt die Liquid Biopsy wie ein Sammelbecken, das die genetischen Informationen des gesamten Körpers bündelt. Sie bietet somit einen repräsentativen Querschnitt über alle aktiven Krankheitsherde.

Die Forschung zur Liquid Biopsy hat in den letzten 36 Monaten enorme Sprünge gemacht. Auf den Fachkongressen der ASCO und ESMO wurden Daten präsentiert, die zeigen, dass Bluttests nicht mehr nur ein Versprechen für die Zukunft sind, sondern bereits heute Leben verlängern können.
Die ENZA-p-Studie: CTCs als Wegweiser zur Radioligandentherapie
Eines der wichtigsten Ergebnisse der Jahre 2024 und 2025 stammt aus der ENZA-p-Studie (ANZUP 1901). Hier wurde untersucht, ob die Kombination des Hormonblockers Enzalutamid mit der neuen Präzisionsbestrahlung Lutetium-177-PSMA-617 ($^{177}$Lu-PSMA) bei Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom (mCRPC) wirksamer ist als die Standardtherapie. Die Liquid Biopsy spielte dabei eine entscheidende Rolle als Biomarker.
In der Studie wurden Patienten untersucht, die eine hohe Anzahl an CTCs aufwiesen. Die Ergebnisse waren eindeutig:
Studienergebnisse: Enzalutamid in Kombination mit Lutetium-177-PSMA-617
Die aktuellen Daten zeigen einen deutlichen Vorteil für Patienten, die die Kombinationstherapie erhielten, im Vergleich zur alleinigen Behandlung mit Enzalutamid:
- Gesamtüberleben (Overall Survival): Auch beim wichtigsten Kriterium, dem Überleben, zeigt sich ein klarer Gewinn. Patienten mit der Kombinationstherapie lebten im Schnitt 34 Monate, während es unter der Standardtherapie mit Enzalutamid allein 26 Monate waren.
- Zeit bis zum PSA-Anstieg (PSA-PFS): Während der PSA-Wert bei der alleinigen Gabe von Enzalutamid bereits nach etwa 7,8 bis 8,0 Monaten wieder anstieg, konnte dieser Zeitraum durch die zusätzliche Gabe von Lutetium-177-PSMA-617 auf 13,0 Monate fast verdoppelt werden.
- Ansprechen des PSA-Werts: Die Chance, dass der PSA-Wert signifikant (um mehr als 50 %) sinkt, war bei der kombinierten Behandlung deutlich höher als bei der alleinigen Hormontherapie.
Besonders interessant: Forscher untersuchten die CTCs auf das Merkmal PSMA und die Resistenzvariante AR-V7. Patienten, bei denen mehr als 50 % der Tumorzellen PSMA-positiv waren, profitierten massiv von der zusätzlichen Lutetium-Therapie. Diese Daten belegen, dass die Analyse von Tumorzellen im Blut direkt vorhersagen kann, welche Patienten von einer teuren und aufwendigen Behandlung wirklich profitieren.
PARP-Inhibitoren und der Nachweis von DNA-Reparaturdefekten
Ein weiterer Schwerpunkt der letzten Jahre war der Einsatz der ctDNA-Analyse zur Identifizierung von Patienten für PARP-Inhibitoren wie Olaparib, Rucaparib oder Niraparib. Diese Medikamente greifen gezielt Zellen an, die ihre eigene DNA nicht mehr reparieren können. Die häufigsten Fehler liegen in den Genen BRCA1, BRCA2 oder ATM. Die FDA und EMA haben mittlerweile Bluttests als Companion Diagnostics zugelassen, um diese Mutationen nachzuweisen, wenn kein frisches Tumorgewebe verfügbar ist.
In der klinischen Praxis bedeutet das: Wenn die Liquid Biopsy eine solche Mutation findet, hat der Patient Zugang zu einer hochwirksamen, zielgerichteten Therapie, die das progressionsfreie Überleben signifikant verlängern kann. Wenn Studiendaten in diesem Zusammenhang als unreif (not mature) bezeichnet werden, bedeutet dies, dass zwar schon ein positiver Trend beim Ansprechen sichtbar ist, aber noch nicht genügend Patienten verstorben sind, um eine endgültige Aussage über das langfristige Gesamtüberleben zu treffen. Dennoch reichen diese „unreifen“ Daten oft schon für eine vorläufige Zulassung aus, da der Nutzen für die Patienten bereits deutlich erkennbar ist.
Nachweis von Resistenzen: Das Beispiel AR-V7
Ein Albtraum für viele Patienten ist der Moment, in dem die gewohnte Hormontherapie (z. B. mit Abirateron oder Enzalutamid) nicht mehr wirkt. Die Liquid Biopsy kann heute die Ursache dafür im Blut finden: die Splice-Variante AR-V7 des Androgenrezeptors. Zellen mit diesem Merkmal haben ihren „Empfänger“ für Hormone so umgebaut, dass die Medikamente nicht mehr andocken können. Studien haben gezeigt, dass Patienten mit AR-V7-positiven Tumorzellen im Blut kaum auf eine weitere Hormontherapie ansprechen, aber weiterhin gut auf eine Chemotherapie mit Taxanen reagieren. Der Bluttest erspart dem Patienten also Monate einer unwirksamen Behandlung und ermöglicht den direkten Wechsel auf eine effektive Alternative.
Wichtig für den Patienten: Kosten, Kassen und Klinikalltag
Der medizinische Nutzen der Liquid Biopsy ist wissenschaftlich belegt, doch der Weg des Patienten zu diesem Test ist in Deutschland oft noch von bürokratischen Hürden geprägt. Es ist wichtig, zwischen Forschung und der täglichen Versorgung zu unterscheiden.
Kassenleistung oder IGeL?
Die Abrechnungssituation für die Liquid Biopsy ist komplex und hängt stark vom Stadium der Erkrankung ab.
Früherkennung: Für die reine Früherkennung ist die Liquid Biopsy derzeit keine Kassenleistung. Der PSA-Test bleibt hier die primäre Methode, die für Männer ab 45 Jahren als IGeL-Leistung (Selbstzahler) angeboten wird. Die Kosten liegen hier zwischen 25 und 50 Euro. Erst bei einem konkreten Verdacht wird der PSA-Test zur Kassenleistung.
Fortgeschrittenes Stadium (mCRPC): Hier übernehmen die gesetzlichen Krankenkassen (GKV) die Kosten für molekulargenetische Untersuchungen oft dann, wenn sie zur Steuerung einer zugelassenen Therapie (z. B. PARP-Inhibitoren) notwendig sind. In vielen Fällen muss der behandelnde Onkologe jedoch einen Kostenübernahmeantrag stellen.
Private Krankenversicherung (PKV): Private Kassen übernehmen die Kosten für innovative Verfahren wie den FoundationOne Liquid CDx oder den Guardant360 CDx in der Regel, wenn eine medizinische Notwendigkeit vorliegt. Eine vorherige Klärung mit der Versicherung wird jedoch dringend empfohlen.
Selbstzahler-Preise: Gezielte Analysen einzelner Mutationen kosten oft zwischen 600 und 700 Euro. Umfassende Genom-Profile aus dem Blut können mehrere tausend Euro kosten.
Wo wird der Test durchgeführt?
Eine Liquid Biopsy ist kein Standardverfahren für das örtliche Hausarztlabor. Patienten sollten sich an spezialisierte Einrichtungen wenden:
Zertifizierte Prostatakarzinomzentren: Diese Zentren, oft an großen Kliniken angesiedelt, verfügen über die notwendige Expertise und Kooperationen mit molekularpathologischen Instituten.
Molekularpathologische Institute: Institute wie die in Penzberg oder spezialisierte Labore in Universitätskliniken (z. B. Düsseldorf, Köln, Dresden) führen die Analysen technisch durch.
Onkologische Schwerpunktpraxen: Erfahrene Onkologen können die Blutentnahme vornehmen und das Material an Speziallabore versenden.
Ab welcher Tumorlast ist der Test sinnvoll?
Die Sensitivität der Liquid Biopsy steigt mit der Menge des Tumorgewebes im Körper. In einem sehr frühen Stadium, wenn der PSA-Wert noch unter 1,5 ng/ml liegt, ist die Menge an zirkulierender Tumor-DNA oft so gering, dass der Test negativ ausfällt, obwohl Krebszellen vorhanden sind. Experten betrachten den Test als besonders aussagekräftig, wenn:
Metastasen in bildgebenden Verfahren (MRT, Knochenszintigrafie) sichtbar sind.
Der PSA-Wert deutlich ansteigt oder bereits über 3-5 ng/ml liegt.
Ein schneller Anstieg des PSA-Wertes (kurze Verdopplungszeit) auf eine hohe biologische Aktivität hindeutet.
Realitäts-Check & Ausblick: Was die Technik (noch) nicht kann
Obwohl die Liquid Biopsy faszinierende Möglichkeiten bietet, darf man sie nicht als unfehlbares „Wundermittel“ missverstehen. Eine ehrliche Bilanz zeigt klare Grenzen auf.
Die Gefahr der falsch-negativen Ergebnisse
Das größte Risiko der Liquid Biopsy ist ein negatives Ergebnis bei tatsächlich vorhandenem Krebs. Man nennt dies falsch-negativ. Da nicht jeder Tumor gleich viel DNA ins Blut abgibt, kann es sein, dass die Analyse schlicht keine Spuren findet. In diesem Fall darf man nicht fälschlicherweise annehmen, man sei geheilt oder gesund. Die Gewebestanze bleibt in solchen Zweifelsfällen weiterhin das sicherste Verfahren.
Clonale Hämatopoese (CHIP)
Ein biologisches Phänomen namens CHIP kann die Ergebnisse verfälschen. Mit zunehmendem Alter entwickeln normale Blutzellen Mutationen, die denen von Krebszellen ähneln. Ein unvorsichtiger Test könnte diese Mutationen als „Prostatakrebs-DNA“ missverstehen. Hochmoderne Labore vergleichen deshalb oft das Blutplasma mit den weißen Blutzellen des Patienten, um solche Fehlerquellen auszuschließen.

In den nächsten Jahren wird sich die Rolle der Liquid Biopsy wandeln.
MRD-Monitoring (Minimal Residual Disease): Nach einer Operation könnten Patienten regelmäßig zum Bluttest gehen. Findet der Test winzige Spuren von ctDNA, noch bevor der PSA-Wert steigt, kann man die Behandlung früher und gezielter wieder aufnehmen.
Therapie-Monitoring: Anstatt alle drei Monate ein CT oder MRT durchzuführen, könnte ein monatlicher Bluttest zeigen, ob die Therapie noch wirkt oder ob sich Resistenzen bilden.
Früherkennung: Auch wenn die S3-Leitlinie (Stand August 2025) aktuell noch auf den PSA-Test und das MRT setzt, könnten kombinierte Blut- und Urintests die Treffsicherheit der Vorsorge in Zukunft massiv erhöhen und viele unnötige Biopsien vermeiden.
 „Das kleine Lexikon“ – Medizinische Begriffe einfach erklärt
„Das kleine Lexikon“ – Medizinische Begriffe einfach erklärt
Apoptose: Der programmierte Zelltod ist ein natürlicher Vorgang, bei dem der Körper alte oder geschädigte Zellen kontrolliert abbaut.
AR-V7: Diese spezielle Variante des Androgenrezeptors macht Krebszellen immun gegen gängige Hormonblocker wie Enzalutamid.
ATM: Ein Gen, das für die Reparatur von DNA-Schäden verantwortlich ist und bei einem Defekt den Einsatz von PARP-Inhibitoren ermöglicht.
Biomarker: Ein messbares Merkmal im Blut oder Gewebe, das Informationen über den Zustand einer Erkrankung oder die Wirksamkeit einer Therapie liefert.
BRCA1/BRCA2: Diese Gene schützen den Körper vor Krebs, indem sie Erbgutschäden reparieren, wobei Mutationen das Risiko für aggressive Krankheitsverläufe erhöhen.
Companion Diagnostic: Hierbei handelt es sich um einen Begleittest, der gesetzlich vorgeschrieben ist, um festzustellen, ob ein Patient für ein bestimmtes Medikament geeignet ist.
ctDNA: Zirkulierende Tumor-DNA sind winzige Erbgutschnipsel, die von absterbenden Krebszellen direkt in das Blut abgegeben werden.
CTCs: Zirkulierende Tumorzellen sind ganze, vom Haupttumor abgelöste Krebszellen, die über den Blutweg neue Metastasen bilden können.
Exosomen: Diese winzigen Bläschen werden von Zellen ausgeschieden und dienen als Botenstoffe, die Erbgut und Proteine durch den Körper transportieren.
FDA / EMA: Die Zulassungsbehörden für Medikamente und Medizinprodukte in den USA beziehungsweise in Europa.
G-BA: Der Gemeinsame Bundesausschuss entscheidet in Deutschland darüber, welche medizinischen Leistungen von der gesetzlichen Krankenkasse bezahlt werden.
Gesamtüberleben (OS): Die statistische Zeitspanne vom Beginn einer Behandlung oder Diagnose bis zum Tod des Patienten.
Heterogenität: Dieser Begriff beschreibt die Tatsache, dass Krebszellen innerhalb desselben Patienten genetisch sehr unterschiedlich beschaffen sein können.
IGeL: Individuelle Gesundheitsleistungen sind medizinische Angebote, deren Kosten der Patient in der gesetzlichen Versicherung selbst tragen muss.
Kastrationsresistent (mCRPC): Ein Stadium des Prostatakrebses, in dem der Tumor trotz eines extrem niedrigen Testosteronspiegels weiterwächst und Metastasen bildet.
Liquid Biopsy: Die Flüssigbiopsie ist ein Verfahren zur Krebsdiagnostik, das Proben aus Körperflüssigkeiten wie Blut oder Urin statt aus festem Gewebe nutzt.
MRD: Die minimale Residualerkrankung bezeichnet kleinste Mengen verbliebener Krebszellen, die nach einer Behandlung im Körper verbleiben und einen Rückfall auslösen können.
NGS: Next-Generation Sequencing ist eine hochmoderne Methode, mit der das gesamte Erbgut einer Zelle in Rekordzeit entschlüsselt werden kann.
PARP-Inhibitor: Eine Medikamentengruppe, die Krebszellen mit Reparaturdefekten daran hindert, ihre DNA zu flicken, was zum Zelltod führt.
Progressionsfreies Überleben (PFS): Die Zeitspanne während oder nach einer Behandlung, in der die Krebserkrankung stabil bleibt und nicht weiter fortschreitet.
PSA-Wert: Das Prostataspezifische Antigen ist ein Eiweiß, dessen Konzentration im Blut Rückschlüsse auf den Zustand der Prostata zulässt.
PSMA: Ein Oberflächeneiweiß der Prostatakrebszelle, das als Zielstruktur für moderne Diagnoseverfahren und radioaktive Therapien dient.
S3-Leitlinie: Ein wissenschaftliches Regelwerk, das Ärzten den aktuell besten Weg für die Diagnose und Behandlung einer Krankheit vorgibt.
Splice-Variante: Eine alternative Form eines Gens, die durch einen anderen Zusammenbau der Erbinformation entsteht und oft zu veränderten Proteinfunktionen führt.
Tumorlast: Die Gesamtmenge des bösartigen Gewebes, das sich zu einem bestimmten Zeitpunkt im Körper des Patienten befindet.
Wichtiger Hinweis und Haftungsausschluss:
Dieser Artikel sowie alle darin enthaltenen Informationen, Daten, Tabellen und Grafiken dient ausschließlich der allgemeinen Information und Aufklärung. Er wurde von einem medizinischen Laien angefertigt und stellt keine medizinische Beratung, Diagnose oder Behandlungsempfehlung dar.
Bitte beachte zudem folgende Punkte:
Kein Ersatz für Fachpersonal: Die Inhalte können und dürfen eine individuelle Untersuchung, Beratung oder Diagnose durch eine qualifizierte medizinische Fachkraft (z. B. Urologe) niemals ersetzen.
Aktualität und Genauigkeit: Die genannten Daten basieren teilweise auf vorläufigen Studienberichten und Schätzungen. Die medizinische Forschung entwickelt sich ständig weiter; daher übernehme ich keine Gewähr für die Richtigkeit, Vollständigkeit oder Aktualität der Inhalte.
Visualisierungen: Grafiken und Tabellen sind als abstrakte, stilisierte Illustrationen zu verstehen. Sie dienen der Veranschaulichung und sind nicht als präzise medizinische Befunddarstellung geeignet.
Solltest du gesundheitliche Beschwerden haben oder medizinische Entscheidungen treffen wollen, konsultiere bitte umgehend einen Arzt.