Der Hoffnungsträger
VIR-5500 (SAR446329 oder auch AMX-500)
Ein verständlicher Leitfaden zum neuen Studienmedikament von Vir Biotechnology gegen fortgeschrittenen Prostatakrebs
Die Behandlung von Prostatakrebs hat in den letzten Jahren enorme Fortschritte gemacht. Dennoch suchen Forscher weltweit nach neuen Wegen für Patienten, bei denen herkömmliche Therapien nicht mehr ausreichend wirken. Ein besonders vielversprechender Kandidat ist das Medikament VIR-5500 (auch bekannt als AMX-500) der Firma Vir Biotechnology. Dieser Artikel erklärt Ihnen einfach und übersichtlich, was hinter dieser neuen Hoffnung steckt.

1.a. Medikamenten-Beschreibung
VIR-5500 ist ein hochmodernes, biologisches Medikament, das man sich wie einen „intelligenten Brückenbauer“ vorstellen kann. Es gehört zu einer neuen Generation von Immuntherapien. Seine Aufgabe ist es, eine direkte Verbindung zwischen den Krebszellen im Körper und den eigenen Abwehrzellen (den T-Zellen) des Immunsystems herzustellen. Normalerweise tarnen sich Krebszellen so geschickt, dass das Immunsystem sie übersieht. VIR-5500 hebt diese Tarnung auf und führt die Abwehrzellen direkt zum Tumor, damit sie diesen bekämpfen können.
1.b. Darreichungsform
Das Medikament wird nicht als Tablette eingenommen, sondern direkt in die Blutbahn verabreicht. Dies geschieht über eine sogenannte intravenöse Infusion (einen „Tropf“). In den aktuellen Studien wird untersucht, ob eine Gabe einmal pro Woche oder einmal alle drei Wochen am besten geeignet ist.
1.c. Medikamenten-Gruppe
VIR-5500 gehört zur Gruppe der „bispezifischen T-Zell-Engager“ (kurz TCE). Das Wort „bispezifisch“ bedeutet, dass das Medikament zwei verschiedene Andockstellen hat: Eine für die Krebszelle (gezielt auf das Eiweiß PSMA) und eine für die Abwehrzelle des Körpers.
1.d. Vergleichbare Medikamente
Obwohl VIR-5500 durch seine spezielle Bauweise einzigartig ist, gibt es andere Medikamente in der Entwicklung, die nach einem ähnlichen Brücken-Prinzip arbeiten. Dazu gehören Wirkstoffe wie Acapatamab oder Pasritamig. Auch die bekannte Radioligandentherapie (wie Pluvicto) zielt auf dieselbe Stelle an der Krebszelle (PSMA) ab, nutzt aber Strahlung statt des Immunsystems zur Bekämpfung.
2. Wirkmechanismus des Medikaments: Das „Trojanische Pferd“
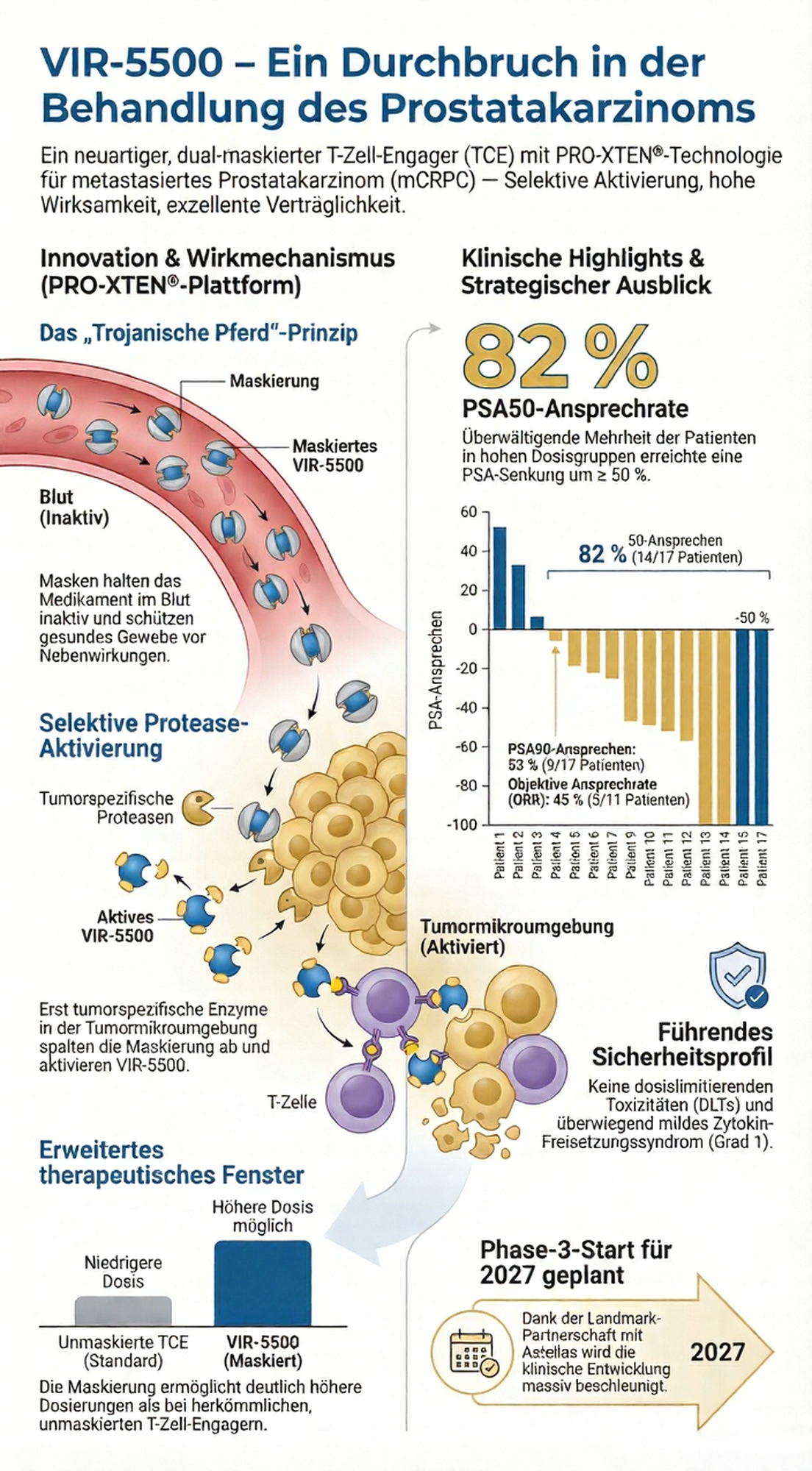
Das Besondere an VIR-5500 ist die sogenannte „Maskierungs-Technologie“ (PRO-XTEN®). Man kann es sich wie ein Trojanisches Pferd vorstellen: Solange das Medikament im gesunden Blutkreislauf schwimmt, ist es durch eine Art Schutzhülle „maskiert“ und damit inaktiv. Das ist wichtig, um Nebenwirkungen im gesunden Körper zu vermeiden. Erst wenn das Medikament direkt in die Umgebung des Tumors gelangt, lösen spezielle Enzyme der Krebszellen diese Maske auf. Erst jetzt wird der Wirkstoff „scharf geschaltet“, aktiviert die Abwehrzellen und gibt den Krebszellen den „Todeskuss“, ohne das gesunde Gewebe unnötig zu belasten.

3. Wahrscheinliche und beobachtete Nebenwirkungen
Wie jedes wirksame Medikament kann auch VIR-5500 Nebenwirkungen haben. Da es das Immunsystem aktiviert, sind die häufigsten Beschwerden ähnlich wie bei einer starken Erkältung oder Grippe.
Zytokin-Freisetzungssyndrom (CRS): Dies ist die bekannteste Reaktion bei dieser Art von Therapie. Etwa die Hälfte der Patienten bekommt kurz nach der Infusion Fieber. In den meisten Fällen war dies jedoch leicht ausgeprägt und gut behandelbar.
Erschöpfung und Müdigkeit: Viele Patienten berichten über eine vorübergehende Schwäche (Fatigue).
Sehstörungen: In sehr seltenen Fällen kam es bei hohen Dosierungen zu verschwommenem Sehen. Die Forscher untersuchen dies aktuell sehr genau, um die Sicherheit weiter zu erhöhen.
Vorteil der Maskierung: Da das Medikament erst im Tumor aktiv wird, konnten schwere Entzündungsreaktionen im restlichen Körper bisher deutlich seltener beobachtet werden als bei älteren, unmaskierten Medikamenten dieser Klasse.

4. Ergebnisse klinischer Studien
4.a. Ergebnisse von vorherigen Studien
Die Entwicklung begann unter dem Namen AMX-500 (später SAR446329 bei der Firma Sanofi). Erste Tests im Labor und in frühen klinischen Phasen zeigten, dass die Maskierung stabil bleibt und das Medikament gezielt am Tumor wirkt. Da das Programm noch relativ jung ist, fließen diese Erkenntnisse direkt in die aktuelle Hauptstudie ein.
4.b. Ausführliche erste Zwischenergebnisse aktueller Studien
Die neuesten Daten vom Februar 2026 sind sehr ermutigend. In der Gruppe von Patienten, die eine höhere Dosis erhielten, zeigten sich beeindruckende Erfolge:
Bei 82 % der Patienten sank der PSA-Wert (ein wichtiger Tumormarker im Blut) um mindestens die Hälfte.
Bei über 50 % der Patienten sank der PSA-Wert sogar um 90 % oder mehr.
In Röntgenbildern konnte bei 45 % der Patienten eine messbare Schrumpfung der Tumore beobachtet werden, sogar bei Absiedlungen in der Leber oder den Lymphknoten.
5. Aktuelle klinische Studien
Die wichtigste laufende Untersuchung ist die internationale Studie mit der Nummer NCT05997615 (auch bekannt als V101-Studie).
5.a. Beschreibung der Studie NCT05997615
Diese Studie ist in verschiedene Abschnitte unterteilt, um das Medikament schrittweise zu prüfen:
Teil 1: Hier wurde die sicherste und wirksamste Dosis für das Medikament allein (Monotherapie) gesucht. Dieser Teil ist bereits weit fortgeschritten.
Teil 3a: Hier wird VIR-5500 in Kombination mit modernen Hormontabletten (wie Enzalutamid oder Darolutamid) getestet. Das Ziel ist es zu sehen, ob die Kombination noch stärker wirkt als das Medikament allein.
Wichtigste Teilnahmebedingungen:
An der Studie können Männer teilnehmen, die an einem metastasierten Prostatakrebs leiden, der nicht mehr auf eine Hormonentzugstherapie anspricht (mCRPC). Meist müssen die Patienten zuvor bereits eine Behandlung mit modernen Hormontabletten oder einer Chemotherapie erhalten haben. Die Studie wird weltweit an verschiedenen Standorten durchgeführt, unter anderem in den USA, Spanien, Großbritannien und Australien.

6. Aktueller Entwicklungsstatus
Das Medikament befindet sich derzeit in der sogenannten Phase 1/2. Das bedeutet, man hat bereits bewiesen, dass es wirkt und welche Dosis sicher ist. Im Jahr 2026 starten nun größere Patientengruppen (Expansionskohorten), um die Ergebnisse zu bestätigen. Ein großer Meilenstein war die Zusammenarbeit mit der Firma Astellas ab Februar 2026, die dabei helfen soll, das Medikament weltweit schneller verfügbar zu machen.
7. Einschätzung der Marktzulassung
Eine Zulassung ist erst möglich, wenn die abschließenden großen Studien (Phase 3) erfolgreich beendet wurden.
7.a. Ausblick USA (FDA)
Die Forscher planen, die entscheidenden Phase-3-Studien im Jahr 2027 zu beginnen. Wenn alles nach Plan läuft, könnte ein Antrag auf Zulassung bei der amerikanischen Gesundheitsbehörde FDA im Jahr 2029 erfolgen.
7.b. Ausblick Europa (EMA)
In Europa erfolgt die Zulassung durch die EMA meist kurz nach oder zeitgleich mit den USA. Wir können daher mit einer möglichen Verfügbarkeit in europäischen Krankenhäusern gegen 2029 oder 2030 rechnen.

8. Aussichten
VIR-5500 ist einer der spannendsten Hoffnungsträger in der aktuellen Krebsforschung. Durch die innovative „Trojanische Pferd“-Technik bietet es die Chance auf eine hochwirksame Zerstörung von Krebszellen bei gleichzeitig besserer Verträglichkeit als frühere Immuntherapien. Besonders für Patienten, bei denen bisherige Standardbehandlungen versagt haben, zeigen die frühen Daten zu PSA-Senkungen und Tumorschrumpfungen ein Potenzial, das viele Experten als „außergewöhnlich“ bezeichnen.
Fazit für Patienten: Obwohl es noch einige Jahre dauern wird, bis das Medikament regulär verschrieben werden kann, ist die Entwicklung sehr dynamisch. Für Patienten in fortgeschrittenen Stadien kann die Teilnahme an einer klinischen Studie bereits heute eine Option sein, um Zugang zu dieser neuen Technologie zu erhalten. Sprechen Sie hierzu am besten mit Ihrem behandelnden Onkologen.
Stand: 04/ 2026
Wichtiger Hinweis und Haftungsausschluss:
Dieser Artikel sowie alle darin enthaltenen Informationen, Daten, Tabellen und Grafiken dient ausschließlich der allgemeinen Information und Aufklärung. Er wurde von einem medizinischen Laien angefertigt und stellt keine medizinische Beratung, Diagnose oder Behandlungsempfehlung dar.
Bitte beachte zudem folgende Punkte:
Kein Ersatz für Fachpersonal: Die Inhalte können und dürfen eine individuelle Untersuchung, Beratung oder Diagnose durch eine qualifizierte medizinische Fachkraft (z. B. Urologe) niemals ersetzen.
Aktualität und Genauigkeit: Die genannten Daten basieren teilweise auf vorläufigen Studienberichten und Schätzungen. Die medizinische Forschung entwickelt sich ständig weiter; daher übernehme ich keine Gewähr für die Richtigkeit, Vollständigkeit oder Aktualität der Inhalte.
Visualisierungen: Grafiken und Tabellen sind als abstrakte, stilisierte Illustrationen zu verstehen. Sie dienen der Veranschaulichung und sind nicht als präzise medizinische Befunddarstellung geeignet.
Solltest du gesundheitliche Beschwerden haben oder medizinische Entscheidungen treffen wollen, konsultiere bitte umgehend einen Arzt.